
电话:+86-755-86967710
邮箱:webmaster@szbl.ac.cn

系统与物理生物学研究所
zhouyq@szbl.ac.cn
AI计算生物学,分子生物学,细胞生物学
资深研究员、副所长
终身正教授
终身正教授
终身副教授
助理教授
Martin Karplus组博士后
Carol Hall组博士后
George Stell组博士后
科学家,实验室主任
化学物理博士
化学物理学士
周耀旗课题组的研究主要是围绕着RNA和蛋白质的序列、结构及功能之间关系的基础研究以及生物高分子的设计、递送、及药物开发的应用研究。课题组研究的特色是干湿结合(结构生物信息计算、AI人工智能深度学习与现代高通量、自动定向进化生物技术相结合)来实现对序列、结构及功能之间关系的深刻理解,从而达到生物高分子在多方面应用的目的,其中包括为精准医疗服务的针对性药物设计、递送和个性化生物标志物的检测。目前的具体项目包括、但不局限于:
1. 后AlphaFold时代的蛋白质结构和功能预测
2. 蛋白质设计和自动定向进化
3. RNA结构预测,RNA语言模型
4. RNA靶向递送
首创利用浅层与深度学习技术实现连续主链二面角预测,使端到端蛋白质结构预测成为可能。这一进展为诺奖工作AlphaFold 2 初步攻克这个分子生物领域长达60年的重大难题奠定了直接基础(图一)。
率先开发人工智能驱动的蛋白质序列设计方法SPIN/SPIN2,实现30–34%的序列恢复率(图二)。该成果被国际权威期刊Current Opinion in Chemical Biology(Ovchinnikov与Huang,2021)评价为机器学习应用于蛋白质设计的起点,标志着该领域研究范式从传统基于能量的方法向人工智能驱动的根本性转变。如今这一范式已主导蛋白质设计领域,推动治疗性蛋白与工业酶设计的革命性进展。
开发了一种新型统计势能RNA-BRiQ,实现了原子级RNA结构优化。该技术赋能AIChemy-RNA2斩获第十五届结构预测关键评估(CASP15,2022年)RNA结构预测冠军。
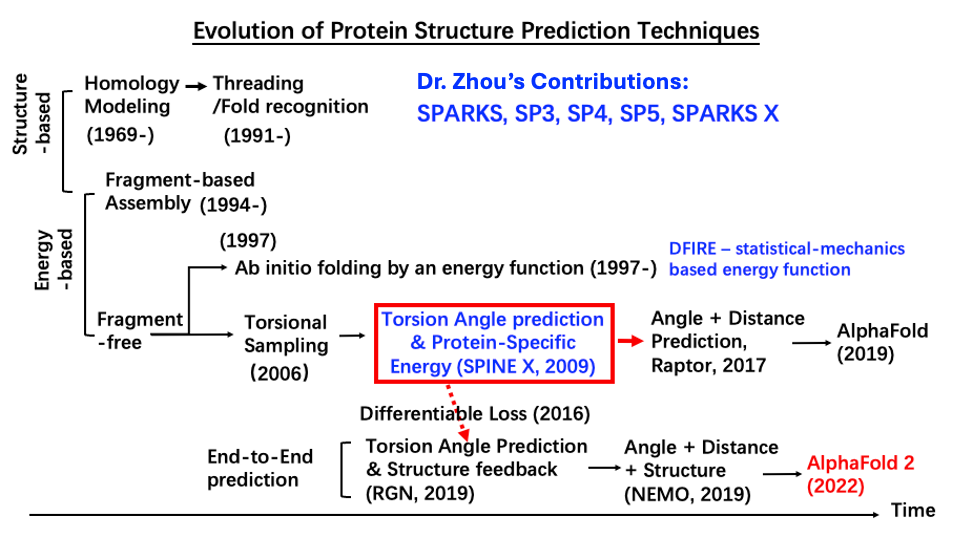
(图一)
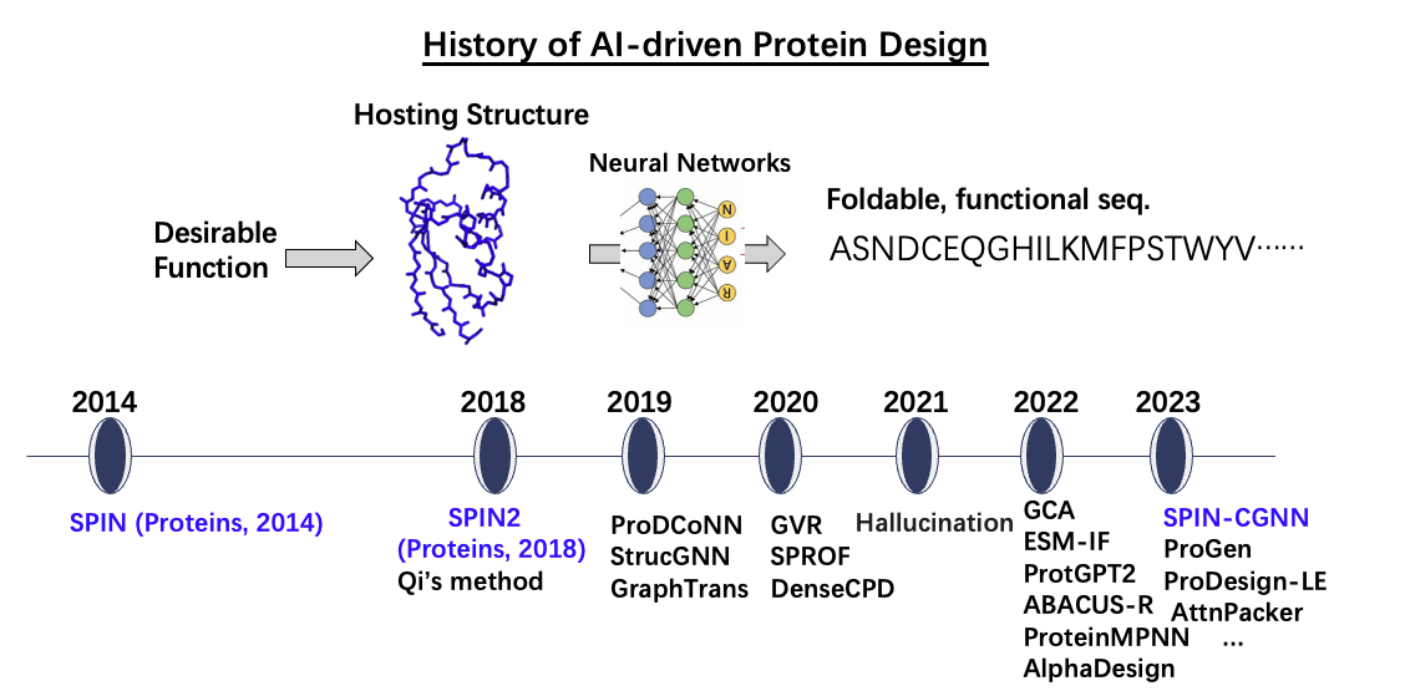
(图二)
1. J. Singh, J. Hanson, K. Paliwal, and Y. Zhou, RNA secondary structure prediction using an ensemble of two-dimensional deep neural networks and transfer learning,Nature Communications10, 5407 (2019).
2. Z. Zhang, P. Xiong, T. Zhang, J. Wang, J. Zhan, and Y. Zhou, Accurate inference of the full base-pairing structure of RNA by deep mutational scanning and covariation-induced deviation of activity,Nucleic Acids Research, 48:1451-1465 (2020).
3. J. Zhan, H. Jia, E. A. Semchenko, Y. Bian, A. M. Zhou, Z. Li, Y. Yang, J. Wang, S. Sarkar, M. Totsika, H. Blanchard, F. E.-C. Jen, Q. Ye, T. Haselhorst, M. P. Jennings, K. L. Seib, and Y. Zhou, Self-derived structure-disrupting peptides targeting methionine aminopeptidase in pathogenic bacteria; a new strategy to generate antimicrobial peptides,FASEB J., 33: 2095–2104 (2019).
4. S. Xu, J. Zhan, B. Man, S. Jiang, W. Yue, S. Gao, C. Guo, H. Liu, Z. Li, J. Wang, and Y. Zhou, Real-time reliable determination of binding kinetics of DNA hybridization using a multi-channel graphene biosensor,Nature Communications8, 14902 (2017).
5. Z. Li, Y. Yang, J. Zhan, L. Dai and Y. Zhou, Energy Functions in De Novo Protein Design: Current Challenges and Future Prospects,Ann. Rev. Biophysics42, 315-335 (2013).
联系方式
地址:深圳市光明区高科创新中心
电话:+86-755-86967710
邮箱:webmaster@szbl.ac.cn
邮编:518132
Copyright © 2025 深圳湾实验室 版权所有www.szbl.ac.cn All Rights Reserved.粤ICP备19032884号 粤公网安备44031102000926号
粤公网安备44031102000926号


